.jpg)
Пузырно-мочеточниковый рефлюкс (ПМР) — это ретроградный заброс мочи из мочевого пузыря в мочеточник и чашечно-лоханочную систему, обусловленный аномалией развития интрамурального отдела мочеточника (при первичном рефлюксе) или повышением внутрипузырного давления вследствие инфравезикальной обструкции или при нейрогенном мочевом пузыре (вторичный рефлюкс) (рис. 1). По данным литературы ПМР встречается приблизительно у 0,4–1,8% детей и является наиболее распространенной аномалией мочевыводящих путей в популяции [1–4]. Основной целью лечения ПМР является предупреждение рецидивирующего течения пиелонефрита, развития повреждений почечной паренхимы, гипертензии и хронической болезни почек.
.jpg)
Последнее десятилетие ознаменовалось значительными изменениями во взглядах на стандарты лечения и ведения детей с пузырно-мочеточниковым рефлюксом (ПМР). Дискутабельными на сегодняшний день являются вопросы эффективности проведения длительной антибактериальной терапии, метода оперативной коррекции рефлюкса и целесообразности лечения рефлюкса как такового [1, 2, 5]. Эндоскопическая коррекция рефлюкса (ЭКР) впервые была предложена в 1981 г. Matouschek Е. как альтернатива консервативной терапии и открытым операциям. В дальнейшем техника была усовершенствована и популяризирована O’Donnell B. и Puri P., которые в 1984 г. опубликовали результаты введения пасты тефлона (subureteric Teflon injection (STING)) [6, 7]. С тех пор с использованием различных имплантатов были пролечены тысячи детей с ПМР.
Повышенный интерес к данному виду лечения был обусловлен рядом важных его преимуществ — малой травматичностью, короткой продолжительностью оперативного вмешательства, возможностью применения в амбулаторных условиях, минимальным риском осложнений, характерных для различных реконструктивно-пластических неоимплантаций мочеточников и отсутствием необходимости длительной антибиотикотерапии.
По данным разных авторов эффективность эндоскопического метода варьирует от 52,4% (Lackgren G., 2002) до 86,7% (Hsieh M., 2010), поэтому считать окончательно решенной эту проблему нельзя. На наш взгляд, результаты эндоскопического лечения зависят от правильно выбранных показаний, техники выполнения процедуры и от используемого имплантата [8–10].
ЭКР проводится при следующих показаниях:
Проанализировав накопленный материал, мы пришли к выводу, что факторами, снижающими эффективность ЭКР, являются полное удвоение верхних мочевых путей и рецидив рефлюкса после реимплантации мочеточника.
Противопоказаниями к использованию метода ЭКР являются следующие условия:
Суть эндоскопической коррекции рефлюкса заключается в восстановлении нарушенной антирефлюксной функции мочеточника путем введения под его выходной отдел жидкого инертного полимера. Полимер формирует бугорок, который после застывания служит жесткой опорой для мочеточника, верхняя стенка которого, плотно прилегая к нижней, обеспечивает клапанную антирефлюксную функцию (рис. 2).
.jpg)
.jpg)
.jpg) Метод ЭКР имеет множество технических нюансов, поэтому и результаты его применения значительно различаются. В настоящее время общепризнанными считаются методики STING, HIT-1 (hydrodistention implantation technique) и HIT-2 (double hydrodistention implantation technique). Основное отличие между ними — место ввода иглы относительно устья мочеточника (рис. 3). Мы используем все виды методик, однако чаще применяем HIT-1 или HIT-2 (рис. 4). По нашему мнению, выбор способа введения необходимо осуществлять с учетом индивидуальных анатомических особенностей устья мочеточника каждого конкретного больного. Всем пациентам инсуфлируется средняя доза имплантата (экспериментально установленная ранее) либо подбор дозы основывается на данных визуального наблюдения за «смыканием устья». Такой субъективизм при проведении ЭКР приводит, на наш взгляд, к снижению эффективности лечения, поскольку если размеры болюса будут недостаточными, длина пузырно-мочеточникового соустья может оказаться меньше необходимой для обеспечения его нормального функционирования. И наоборот, размеры болюса, превышающие предельно допустимые, могут привести к тому, что анатомические структуры области устья мочеточника могут оказаться не в состоянии удерживать такой болюс в фиксированном положении. Последнее приводит к смещению введенного имплантата и отслаиванию слизистой оболочки с нарушением кровоснабжения зоны манипуляции. В результате развивается воспалительная реакция в области имплантации с возможностью последующего образования дефекта, а также отторжения и, следовательно, рецидива ПМР.
Метод ЭКР имеет множество технических нюансов, поэтому и результаты его применения значительно различаются. В настоящее время общепризнанными считаются методики STING, HIT-1 (hydrodistention implantation technique) и HIT-2 (double hydrodistention implantation technique). Основное отличие между ними — место ввода иглы относительно устья мочеточника (рис. 3). Мы используем все виды методик, однако чаще применяем HIT-1 или HIT-2 (рис. 4). По нашему мнению, выбор способа введения необходимо осуществлять с учетом индивидуальных анатомических особенностей устья мочеточника каждого конкретного больного. Всем пациентам инсуфлируется средняя доза имплантата (экспериментально установленная ранее) либо подбор дозы основывается на данных визуального наблюдения за «смыканием устья». Такой субъективизм при проведении ЭКР приводит, на наш взгляд, к снижению эффективности лечения, поскольку если размеры болюса будут недостаточными, длина пузырно-мочеточникового соустья может оказаться меньше необходимой для обеспечения его нормального функционирования. И наоборот, размеры болюса, превышающие предельно допустимые, могут привести к тому, что анатомические структуры области устья мочеточника могут оказаться не в состоянии удерживать такой болюс в фиксированном положении. Последнее приводит к смещению введенного имплантата и отслаиванию слизистой оболочки с нарушением кровоснабжения зоны манипуляции. В результате развивается воспалительная реакция в области имплантации с возможностью последующего образования дефекта, а также отторжения и, следовательно, рецидива ПМР.
Сегодня в клинической практике используется широкий спектр препаратов для ЭКР. Все они должны отвечать следующим требованиям: быть биологически совместимыми с тканями организма человека, безопасными и не мигрировать в другие ткани и органы.
Применяемые имплантаты можно разделить на две группы: нестабильные (рассасывающиеся) и стабильные (нерассасывающиеся). В последние пять лет в нашей клинике предпочтение отдается стабильным имплантатам Уродекс и Вантрис.
Уродекс (Urodex) представляет собой суспензию микрочастиц декстраномера (DEAE Сефадекс) и поперечно сшитых молекул гиалуроновой кислоты неживотного происхождения. Именно поперечно сшитые молекулы гиалуроновой кислоты и являются транспортным средством для микрочастиц декстраномера. Проведенные исследования показали, что Уродекс оказывает стимулирующее действие на соединительную ткань в месте инъекции, за счет возобновления синтеза волокон коллагена в ткани. Уродекс не токсичен, не карциногенен, не мигрирует в ткани и органы [11–14]. Через несколько лет он распадается на воду и углекислоту.
По собственным результатам использования Уродекса в период с 2008 по 2010 г. эффективность его применения составила 84,4%.
Вантрис (Vantris) представляет собой гидрогель синтетического происхождения, неабсорбируемое биологически совместимое объемообразующее вещество, разработанное компанией Promedon (Аргентина). Вантрис представляет собой макрочастицы cополимера полиакрилового и поливинилового спирта, диспергированного в 40%-ном растворе глицерина. После имплантации Вантриса глицерин полностью элиминируется ретикулоэндотелиальной системой и экскретируется почками в неизмененном виде, в то время как частицы кополимера осуществляют перманентную тканевую аугментацию. Размеры частиц Вантриса (90–1000 мкм, большинство из которых > 300 мкм) обуславливают отсутствие миграции. Частицы Вантриса имеют неправильную форму, эластичны и легко принимают необходимый вид, что позволяет свободно инсуфлировать гель через иглу 23-го калибра. Частицы выдерживают тканевые изменения температуры и кислотности [15, 16].
В 2011 г. в нашем отделении было пролечено 43 ребенка в возрасте от 7 месяцев до 13 лет (средний возраст 1,6 года) с ПМР II–V степени. У 14 больных ПМР был двусторонним, у 29 — односторонним (всего 57 мочеточников).
ПМР II степени был у 11 детей (25,6%), III степени — у 19 (44,1%), IV степени — у 9 (20,9%), 5 степени — у 4 больных (13,9%).
Эндоскопическая коррекция проводилась по стандартной методике, принятой в клинике (STING или HIT). Количество вводимого имплантата определялось индивидуально и варьировало от 0,4 до 0,9 мл. Всем детям в послеоперационном периоде проводилось ультразвуковое сканирование почек и мочевого пузыря, при котором оценивались размеры чашечно-лоханочной системы, мочеточника и размеры и локализация болюса имплантата. Контрольное ультразвуковое исследование проводилось через 1,3 и 6 месяцев, результат коррекции рефлюкса оценивался по данным микционной цистоуретрографии через 6 месяцев, статическая сцинтиграфия выполнялась через 1 год после оперативного лечения.
По данным микционной цистографии, проведенной через 5–10 месяцев после процедуры эндоскопической коррекции ПМР, рефлюкс не определялся в 46 мочеточниках (80,7% случаев), снижение степени рефлюкса до I–II отмечалось в 7 случаях (12,2%), эффекта не было (отрицательный результат) в 4 случаях (7%), при этом у 2 детей возникшая после введения Вантриса дилатация чашечно-лоханочной системы и мочеточника сохранялась в течение 6 месяцев и послужила поводом для неоимплантации мочеточников, у 2 детей степень рефлюкса сохранялась на прежнем уровне.
У всех пациентов в послеоперационном периоде зафиксировано более благоприятное течение пиелонефрита, по результатам проведенной статической сцинтиграфии почек через 8–12 месяцев (30 детей) признаков прогрессирования нефросклероза не отмечено.
Суммируя все вышесказанное, еще раз отметим, что наиболее надежные результаты эндоскопической коррекции ПМР можно получить в случае проведения правильной техники процедуры опытным хирургом. Эффективность ЭКР зависит от степени рефлюкса и первичности процедуры, т. к. неправильно выполненная предыдущая манипуляция резко снижает эффективность лечения из-за того, что устье мочеточника фиксируется в невыгодном положении. На результат ЭКР влияют грубые аномалии устья мочеточника и дисфункции мочевого пузыря. Мы убеждены, что при использовании нерассасывающихся паст Уродекс и Вантрис можно получить высокий процент излечения пузырно-мочеточникового рефлюкса.
Литература
С. Н. Зоркин, доктор медицинских наук, профессорС. А. Борисова, кандидат медицинских наук
ФГБУ НЦЗД РАМН, Москва
Контактная информация об авторах для переписки: [email protected]
www.lvrach.ru
 Пузырно-мочеточниковый рефлюкс у детей( ПМР )– это обратный ток мочи от мочевого пузыря к мочеточнику и почечной лоханке. Рефлюкс встречается у 1–2% детей, среди детей с пиелонефритом – у 25–40%, и выявляется в 70% случаев в возрасте до 1 года, в 25% случаев – в возрасте 1–3 лет, в 15% случаев – в возрасте 4–12 лет, в более старшем возрасте – в 5% случаев. В течение первого года жизни заболевание значительно чаще выявляется у мальчиков, чем у девочек, в более старшем возрасте отмечается обратное соотношение.
Пузырно-мочеточниковый рефлюкс у детей( ПМР )– это обратный ток мочи от мочевого пузыря к мочеточнику и почечной лоханке. Рефлюкс встречается у 1–2% детей, среди детей с пиелонефритом – у 25–40%, и выявляется в 70% случаев в возрасте до 1 года, в 25% случаев – в возрасте 1–3 лет, в 15% случаев – в возрасте 4–12 лет, в более старшем возрасте – в 5% случаев. В течение первого года жизни заболевание значительно чаще выявляется у мальчиков, чем у девочек, в более старшем возрасте отмечается обратное соотношение.
пузырно мочеточниковый рефлюкс ПМР (пузырно-мочеточниковый рефлюкс ) вызывает нарушение оттока из верхних мочевых путей, что нарушает пассаж мочи и создаёт благоприятные условия для развития воспалительного процесса (пиелонефрит ), рубцеванию почечной паренхимы с развитием рефлюкс-нефропатии, артериальной гипертензии и хронической почечной недостаточности.
Обратный (ретроградный) ток мочи из мочевого пузыря в мочеточник является следствием несостоятельности клапанного механизма уретеро-везикального(пузырно-мочеточникового) сегмента(УВС).
Н.А.Лопаткин выделяет 3 группы теорий развития рефлюкса: первая заявляет главной причиной порок развития пузырно-мочеточникового сегмента, вторая говорит о формировании несостоятельности уретеро-везикального соустья как следствие воспалительного процесса с последующей фибропластической трансформацией, сторонники третьей теории считают главной причиной нарушение нервного аппарата мочеточника.
Выделяют первичный пмр, причиной которого является врожденная аномалия развития – укорочение внутрипузырного отдела мочеточника. Первичный рефлюкс может быть наследственно обусловленным. С ростом и развитием ребенка происходит «дозревание» структур, формирующих клапанный механизм, в связи с чем возможна спонтанная регрессия рефлюкса. Замечено, что чем выше степень рефлюкса – тем меньше вероятность его самостоятельного исчезновения. Несостоятельность клапанного механизма УВС отмечается аномалии расположения устья мочеточника – дистопии, эктопии.
Причины вторичного пмр – повышение внутрипузырного давления (клапан задней уретры, различные варианты дисфункции мочевого пузыря), хронический цистит. Хронический воспалительный процесс приводит к склеротическим изменениям в области уретеровезикального сегмента, укорочению интрамурального отдела мочеточника и зиянию устья. В свою очередь, хронический цистит нередко возникает и поддерживается инфравезикальной обструкцией.
Повреждение почечной паренхимы при ПМР происходит как вследствие повторения (рецидивирования) инфекционного процесса, так и вследствие «гидродинамического удара». Аномальная закладка мочеточника, приводящая к дистопии или эктопии устья, влечет за собой формирование диспластичной почки, что также отражается на ее функции.
Пузырно-мочеточниковый рефлюкс подразделяется на пассивный, возникающий в фазу наполнения, активный, возникающий в момент мочеиспускания и пассивно-активный или смешанный. Выделяют интермиттирующий пузырно-мочеточниковый рефлюкс, не доказанный рентгенологическими методами, но имеющий характерную клиническую картину – рецидивирующий пиелонефрит, периодическая лейкоцитурия, косвенные ультразвуковые и рентгенологические признаки пузырно-мочеточникового рефлюкса.
Наиболее распространенной является классификация, предложенная P.E.Heikkel и K.V.Parkkulainen в 1966 году, адаптированная в 1985 году International Reflux Study Group. В зависимости от уровня заброса контрастного вещества и степени расширения мочеточника и собирательной системы почки, выявленных при ретроградной цистоуретрографии, выделяют 5 степеней ПМР:
I степень – обратный заброс мочи из мочевого пузыря только в дистальный отдел мочеточника без его расширения;
II степень – заброс мочи в мочеточник, лоханку и чашечки, без дилатации и изменений со стороны форниксов;
III степень – обратный заброс мочи в мочеточник, лоханку и чашечки при незначительной или умеренной дилатации мочеточника и лоханки и склонности к образованию прямого угла форниксами;
IV степень – выраженная дилатация мочеточника, его извилистость, дилатация лоханки и чашечек, огрубленность острого угла форниксов при сохранении сосочковости у большинства чашечек;
V степень – выраженная огрубленность острого угла форниксов и сосочков, дилатация и извилистость мочеточника.
Ряд авторов использует понятие «мегауретер» при диаметре расширенного мочеточника более 7 мм, при наличии рефлюкса говорят о «рефлюксирующем мегауретере».
Клиническая картина. Жалобы, симптомы.
Пузырно-мочеточниковый рефлюкс у детей не имеет специфической клинической картины, течение заболевания у детей, особенно раннего возраста, как правило бессимптомно.
Жалобы обычно возникают при манифестации пиелонефрита. Отмечается повышение температуры до фебрильных цифр, диспептические явления, боли в животе, признаки интоксикации, помутнение мочи. Дети старшего возраста жалуются на боли в поясничной области после мочеиспускания. При бессимптомном течении наличие рефлюкса можно заподозрить при проведении скринингового ультразвукового исследования почек (пре- и постнатально). Показанием к проведению полного комплекса урологического обследования является расширение лоханки (поперечный размер – более 5 мм) и мочеточника, косвенным признаком рефлюкса при УЗИ считается нарастание расширения собирательной системы почки и мочеточника по мере наполнения мочевого пузыря.
Основным методом диагностики пузырно-мочеточникового рефлюкса у детей является ретроградная цистоуретрография.
Исследование необходимо выполнять не ранее чем через неделю после купирования воспалительного процесса, т.к. воздействие токсинов на мочеточник может исказить истинную картину состояния мочеточников.
Для определения причины пмр, оценки функции почки и выявления склеротических изменений в почечной паренхиме обязательно проведение комплексного обследования, включающего: ультразвуковое исследование почек с допплерографической оценкой показателей внутрипочечного кровотока и мочеточниково-пузырных выбросов, исследование уродинамики нижних мочевых путей (ритм спонтанных мочеиспусканий, цистометрия или видеоцистометрия, урофлоуметрия), также применяются лучевые методы – внутривенная экскреторная урография, динамическая радиоизотопная ренография (технеций-99), статическая радиоизотопная ренография (DMSA).
Основной целью лечения рефлюкса детей является предотвращение развития рефлюкс-нефропатии, для чего необходимо исключить два основных повреждающих фактора – «гидродинамический удар» и рецидивирование инфекционного процесса. Лечение вторичного рефлюкса должно быть направлено на устранение вызвавших его причин.
При любой степени рефлюкса показано проведение консервативных мероприятий, включающих:
– Коррекцию метаболических нарушений в нервно-мышечных структурах мочеточника и мочевого пузыря (элькар, пикамилон, гипербарическая оксигенация, физиотерапевтические процедуры).
– Профилактику и лечение инфекции мочевых путей (уросептики, антибактериальная терапия, иммунокоррекция, фитотерапия).
– Устранение имеющихся нарушений уродинамики на уровне нижних мочевых путей.
Чем меньше частота рецидивов пиелонефрита, тем ниже риск развития рефлюкс-нефропатии, что оправдывает применение антимикробных препаратов у пациентов с ПМР.
После проведённого курса лечения через 6–12 мес. выполняют контрольную цистографию. Эффективность консервативного лечения при I–III степени пузырно-мочеточникового рефлюкса составляет 60–70%, у детей раннего возраста – до 100%.
Показания к оперативному лечению рефлюкса должны определяться с учетом возраста ребенка и причины рефлюкса.
Учитывая возможность спонтанной регрессии рефлюкса у детей первого года жизни необходимо придерживаться максимально консервативной тактики. При высоких степенях рефлюкса, а также неадаптированном мочевом пузыря предпочтительно выполнение эндоскопической коррекции рефлюкса. К оперативному лечению следует прибегать при только при выявлении аномалии положения устья мочеточника (дистопия, эктопия).
У детей старшего возраста возможность спонтанного исчезновения рефлюкса значительно ниже. При первичном рефлюксе предпочтительна эндоскопическая или оперативная коррекция.
- Рецидивирование инфекции мочевых путей несмотря на антимикробную профилактику
- Сохранение рефлюкса после коррекции дисфункций мочевого пузыря
- Неэффективность консервативного лечения (отсутствие роста или прогрессирование сморщивания почки, снижение функции почки)
- Рефлюкс в сочетании с другими аномалиями развития (удвоение мочеточника, дивертикул мочевого пузыря и т.п.)
Проводится путем имплантации какого-либо вещества в подслизистом отделе устья мочеточника с целью усиления пассивного компонента клапанного механизма. Среди преимуществ метода – малая инвазивность и возможность повторных манипуляций в области УВС. Недостатками метода являются невозможность интраоперационной оценки эффективности созданного клапанного механизма, миграция или деградация введенного препарата с течением времени, что может привести к необходимости повторной манипуляции. В качестве имплантируемого вещества предложены различные материалы – ауто- и гетерологичные. Идеального вещества для подслизистой имплантации в нестоящее время не существует, наиболее широкое распространение получили коллаген, уродекс (urodex), вантрис (vantris), каждый из которых, в свою очередь, имеет свои особенности.
Общим принципом оперативной коррекции является создание клапанного механизма уретеро-везикального соустья за счет формирования подслизистого тоннеля достаточной длины, соотношение между диаметром мочеточника и длиной тоннеля должно быть не менее 1:5. Наиболее распространенными являются операции Политано-Леадбеттера, Коэна, Гленн-Андерсона, Жиль-Вернэ, Лих-Грегуара.
В послеоперационном периоде необходим контроль за размерами почки, собирательной системы и мочеточников, а также проведение антимикробной профилактики. Рентгеновское исследование для оценки эффективности операции проводится через 3–6 месяцев.
При вторичном рефлюксе лечение направлено на устранение факторов, провоцирующих его возникновение.
При наличии клапана задней уретры производится трансуретральная резекция створок клапана с последующим дренированием мочевого пузыря через уретральный катетер и/или цистостому. Решение вопроса о необходимости дальнейшего дренирования проводится после контрольной уретроскопии через 10 дней, при условии сокращения диаметра мочеточников и собирательной системы почек.
При наличии дисфункции нижних мочевых путей лечение осуществляется в зависимости от типа выявленных нарушений.
При низких степенях рефлюкса (I–III), отсутствии выраженных изменений со стороны почечной паренхимы и рецидивов пиелонефрита возможно полное излечение без каких-либо последствий.
При образовании участков склероза в почечной паренхиме говорят о развитии рефлюкс-нефропатии.
Рефлюкс IV–V степени в 50–90% сопровождается врожденным повреждением паренхимы почки, связанным с ее дисплазией или вторичным сморщиванием.
По данным последних исследований стерильный рефлюкс не приводит к развитию рефлюкс-нефропатии. Наибольшее повреждение паренхимы почки происходит при первом эпизоде пиелонефрита. При рецидивировании инфекционного процесса вероятность развития сморщивания почки возрастает в геометрической прогрессии. У детей первого года жизни риск развития сморщивания почки значительно выше, чем у детей более старшего возраста.
Всем детям с пузырно-мочеточниковым рефлюксом необходимо динамическое наблюдение уролога и нефролога.
Необходим контроль общего анализа мочи 1 раз в 2-3 недели, общего анализа крови раз в 3 месяца, биохимического анализа крови и мочи (1 раз в 6 месяцев), ультразвуковое исследование почек 1 раз в 3-6 месяцев, радиоизотопное исследование почек 1 раз в год, цистография – после проведения курса терапевтического лечения, через 1 год с целю оценки регрессии рефлюкса. Необходимость антимикробной профилактики у детей с I–III степенью рефлюкса решается в зависимости от изменений в общем и микробиологическом анализе мочи. При IV–V степени антимикробная профилактика должна проводится непрерывно.
xn--80afoc1aneiwm2i.xn--p1ai
Если у ребенка имеется пузырно мочеточниковый рефлюкс, следует обязательно лечить данное заболевание, в противном случае можно получить необратимые изменения в почке с потерей ее функции! Современное лечение ПМР включает в себя комплекс мероприятий (терапевтических и хирургических), направленных на устранение причины рефлюкса и ликвидацию его последствий. Для выбора верной тактики лечения необходимо тщательное обследование ребенка. Основным методом диагностики ПМР является микционная цистография - рентгенологическое исследование наполненного контрастным веществом мочевого пузыря. При цистоскопии по состоянию устьев мочеточников уточняется форма рефлюкса.
Детские урологи медцентра "МедикаМенте" накопили большой опыт лечения детских урологических заболеваний и готовы помочь Вашему ребенку. Специализированный детский хирургический стационар в Королеве оснащен современной медицинской аппаратурой, а детские хирурги Центра мастерски владеют современными методиками в области урологической эндоскопии. Дети, поступающие в стационар МедикаМенте с диагнозом пузырно-мочеточниковый рефлюкс, проходят лечение лично у главного врача клиники - к.м.н., детского уролога-андролога с большим опытом и стажем Никитского М.Н.
Хирургические операции при ПМР у детей имеют 2 основные разновидности. Это традиционная пересадка мочеточника (выполняемая лапароскопически или через разрез в области живота на открытом мочевом пузыре) и эндоскопическая коррекция рефлюкса. В случае необходимости операции хирург медцентра МедикаМенте отдает предпочтение наиболее современным и малотравматичным методам лечения, а именно: эндоскопической коррекции пузырно-мочеточникого рефлюкса у ребенка. В нашем центре можно выполнить подслизистую имплантацию любого объемобразующего препарата (Vantris, Urodex). Однако следует понимать, что выбор метода лечения зависит от множества факторов и проводится индивидуально в каждом конкретном случае. В ряде случаев (при высоких степенях рефлюкса, после неудачных инъекционных эндоскопических коррекций) предпочтение может быть отдано традиционной антирефлюксовой операции на открытом мочевом пузыре.
(*нам важно Ваше мнение о наших услугах)
В любом возрасте оперативное лечение пузырно-мочеточникового рефлюкса у детей выполняется под наркозом. Маленький пациент засыпает, а когда просыпается, все неприятности уже позади. Использование анестетика последнего поколения Севоран делает выход из наркоза и возвращение к нормальному состоянию достаточно скорым и комфортным. В центре детской хирургии "МедикаМенте" по согласованию с хирургом мама или папа могут находиться рядом с ребенком в операционной, пока он не уснет от наркоза.
Высокий уровень сервиса в стационаре клиники "Медика Менте" и возможность совместного пребывания с ребенком делают процесс лечения максимально комфортным для родителей и юного пациента. Комфортабельные одно- и двухместные палаты оснащены импортной медицинской мебелью, отдельным санузлом, телевизором, беспроводным интернетом (Wi-Fi). Каждая кровать в стационаре оснащена кнопкой «вызов» для связи с медперсоналом. Питание для пациентов стационара организовывается в индивидуальном режиме ...фото палат стационара
Часто бывает что, что операцию пузырно-мочеточникового рефлюкса в стационаре городской больницы приходится ждать в очереди несколько месяцев. Госпитализация в стационар клиники МедикаМенте осуществляется в удобное для вас время и в кратчайшие сроки ...как происходит госпитализация
Эндоскопическая коррекция ПМР отличается минимальной травматичностью и коротким сроком госпитализации. Как правило, через 2-4 часа после операции состояние пациента полностью нормализуется. Через сутки после проведения контрольного УЗИ в случае удовлетворительного состояния дети выписываются под амбулаторное наблюдение.
Открытое оперативное лечение пузырно-мочеточникового рефлюкса – достаточно серьезная операция. Длительность оперативного вмешательства составляет не менее полутора часов. Операция выполняется под эндотрахеальным наркозом, требует разреза в нижней части живота, пребывания в больнице (продолжительность неосложненного госпитального периода после полостной операции составляет в среднем от 7 суток), катетеризации пузыря после операции. Открытая операция рекомендуется, в основном, для лечения высоких степеней рефлюкса с нарушением анатомии устья мочеточника.
Эндоскопическая коррекция является альтернативой оперативному лечению пузырно-мочеточникового рефлюкса. В отличие от операции на открытом мочевом пузыре при эндоскопическом методе процедура занимает 30-40 минут, не оставляет шрамов, отличается меньшими послеоперационными осложнениями и сводит к минимуму период госпитализации и восстановления. Как правило, через 2-4 часа состояние пациента полностью нормализуется. Через сутки ребенок выписывается под амбулаторное наблюдение.
Метод обладает малой инвазивностью. Коррекция ПМР проводится с помощью прибора эндоскопа под кратковременным ингаляционным (масочным) наркозом. Используются современные детские (очень тонкие) операционные цистоскопы фирмы «STORZ» (Германия). В место, где мочеточник входит в мочевой пузырь, вводится специальный гель, препятствующий возвращению мочи в мочеточник. Используемый имплантат (объемобразующий гель) имеет огромное значение в эндоскопической методике лечения рефлюкса мочевого пузыря у детей. В стационаре МедикаМенте для эндоскопической коррекции пузырно-мочеточникового рефлюкса используются современные высокоэффективные препараты зарубежного производства. До 85% больных избавляются от ПМР после первой процедуры. Контрольная цистография выполняется через 6 месяцев.
Пройти предоперационное обследование можно в поликлинике по месту жительства или в любой коммерческой клинике. Сканы результатов анализов необходимо прислать на наш электронный адрес. Перед операцией необходимо будет предоставить оригиналы анализов, выписок и заключений врачей. Уточняйте у своего лечащего врача список анализов и обследований перед операцией, так как в некоторых случаях при сопутствующей патологии необходимы дополнительные консультации и обследования.
deti.medmente.ru
Под пузырно-мочеточниковым рефлюксом подразумевается ретроградный ток мочи из мочевого пузыря в мочеточник и почку. В 1898 году Young установил, что ПМР не возникает в нормальном мочевом пузыре. Работы Hutch и Hodgson 1957 выявили связь ПМР и инфекции мочевых путей и рубцевание почечной паренхимы на фоне обострений пиелонефрита и открыли современный этап в лечении рефлюкса.
Для понимания причин возникновения ПМР необходимо представить анатомические компоненты нормального пузырно-мочеточникового соустья (Рис.1), а также аномалии, наиболее часто играющие роль в генезе ПМР Sheldon (1997).
| Рис.1 Основные причины возникновения ПМР |
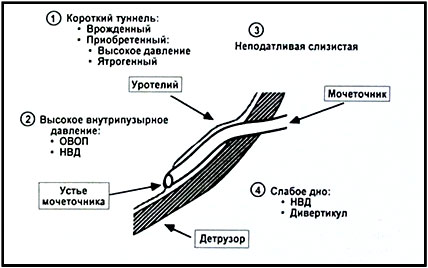 |
| НВД –нейровезикальная дисфункция ОВ0П- инфравезикальная обструкция |
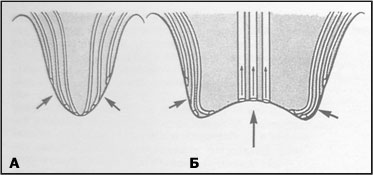
Нормальное пузырно-мочеточниковое соустье характеризуется наличием косо расположенного устья мочеточника и определенной протяженностью подслизистой части мочеточника (зависит от возраста), длина которой значительно превышает диаметр мочеточника. Подобная анатомическая конфигурация обеспечивает работу соустья по типу пассивного клапанного механизма Tanagho 1965,King 1974. По мере наполнения мочевого пузыря и повышения внутрипузырного давления стенка пузыря растягивается, оказывая воздействие на «крышу» верхнюю часть мочеточникового туннеля. В результате мочеточник сдавливается, его просвет закрывается, и таким образом возникает препятствие ретроградному току мочи (Рис.2).
| Рис.2 Механизм возникновения ПМР |
 |
| А. длинный подслизистый туннель, моча внутри пузыря сдавливает просвет мочеточника ( внутрипузыр-ного подслизистого отдела) и препятствует рефлюксу Б. короткий подслизистый туннель нет антирефлюкс-ного механизма. |
Периодическое повышение внутрипузырного давления, например во время мочеиспускания, при физической нагрузке, в вертикальном положении, при кашле, немедленно вызывает сопротивление обратному току мочи. Этот эффект дополняется активным сокращением мышц в области мочепузырного треугольника (Льето) и перистальтикой мочеточника Stephens (1962), Ecksman (1966).
Короткий подслизистый туннель, воспалительные изменения слизистой мочевого пузыря, высокое внутрипузырное давление (нейрогенные расстройства мочевого пузыря), сужения уретры, фимоз и др.) способствуют возникновению рефлюкса. Появлению рефлюкса могут содействовать слабость детрузора (атония, пороки позвоночника - спинальный мочевой пузырь), анатомические дефекты мочевого пузыря (дивертикул, уретероцеле). Однако с возрастом подслизистый отдел мочеточника имеет тенденцию к удлинению и предрасположенность к рефлюксу может исчезнуть King (1974).
Принципиально важное значение имеет понятие интраренального рефлюкса (ИРР) – обратный заброс мочи в чашечках через канальцы в ткань почки. существование ИРР установлено как клинически Rolleston (1974) так и экспериментально Hodgson (1975) (Рис.3).
 |
| Рис.3 Схема интраренального рефлюкса. |
А.Обычное косое расположение устьев собирательных канальцев при их впадении в простые сосочки препятствует ИРР, в то время как конфигурация устьев, впадающих в сложные сосочки (Б) , способствует возникновению рефлюкса. Давлением критическим для возникновения ИРР, считается 35мм Нg в сложных сосочках Thomsen (1982).В эксперименте такое давление может вызывать образование рубцов даже при отсутствии инфекции Hodson CJ (1975), Heptinstall RH (1984). Если в мочевом пузыре давление поднимается до указанного уровня, то это несет в себе риск поражения почек. Для того же, чтобы вызвать интраренальный рефлюкс в простых сосочках, нужно более высокое давление.
Сочетание инфекции и ИРР обладает особенно разрушительным действием. Развитие форникального рубцевания объясняется различной чувствительностью ренальных сосочков к ИРР. Распределение сложных сосочков на полюсах почек четко соответствует преимущественному образованию рубцов в верхнем и нижнем полюсах С.A.Sheldon (1998).
Виды ПМР очень разнообразны, что обусловило многочисленные попытки создания классификаций. Выделялся рефлюкс низкого давления (пассивный) – возникающий во время наполнения мочевого пузыря при микционной цистоуретрографии и высокого давления (активный) – только во время мочеиспускания. Рефлюкс обусловленный врожденной недостаточностью пузырно-мочеточникового сегмента, считают первичным, а развивающийся на фоне обструкции (клапан задней уретры, меатостеноз, стеноз уретры) или нейрогенной дисфункции мочевого пузыря – вторичным. Кроме того принято разделять рефлюкс на простой и осложненный, при этом к осложненному относят рефлюксирующий мегауретер, рефлюксирующий мочеточник при дивертикуле или уретероцеле и редкие случаи сочетания рефлюксирующего мочеточника с ипсилатеральной (с той же стороны) обструкцией пиелоуретрального сегмента или пузырно-мочеточникового сегмента. Однако большинство наиболее распространенных классификаций основано на количественной оценке степени рефлюкса Levitt SB (1981), В настоящее время применяется международная классификация рефлюкса по степени, представленная (на Рис.4) Dwoskin JY (1973).
| Рис.4. Международная классификация ПМР |
 |
1ст. заброс мочи в нижнюю треть мочеточника
2ст. рефлюкс до лоханки
3ст. рефлюкс до лоханки с расширением ЧЛС
4ст. рефлюск с деформацией форниксов и изгибами мочеточника
5ст. рефлюкс с резким расширением мочеточника.ЧЛС и снижением функции почки
В этой классификации учитывается не только уровень обратного тока мочи и наличие расширения мочеточника и почечной лоханки, но также и возникающие в результате рефлюкса анатомические изменения свода чашечек.
При Iст. ПМР на цистограммах визуализируется нерасширенный мочеточник, в то время как при IIст. степени – не только мочеточник, но и нерасширенные почечная лоханка и чашечки. При рефлюксе IIIст. имеется легкое или умеренное расширение или изгибы мочеточника, а также легкое или средней степени расширение почечной лоханки и чашечек. Своды, однако, остаются заостренными или минимально закругленными. Как только углы сводов полностью закругляются, развивается IV степень рефлюкса, при этом сосочки в большинстве чашечек могут еще визуализироваться. Исчезновение сосочков вместе с увеличением расширения и изгибов расценивается как V степень рефлюкса.
Диагностика ПМР проводится с помощью МЦУГ (микционной цистоуретрографии) с контрастным веществом или изотопом. Большую осторожность следует соблюдать, чтобы избежать возникновения или усиления рефлюкса в связи с техническими особенностями проведения обследования. Контрастное вещество, не слишком концентрированное, следует нагревать до температуры тела ребенка. Контраст вводят в мочевой пузырь через тонкий катетер под умеренным давлением, медленно, без анестезии. Объем вводимой жидкости зависит от возраста ребенка. Целесообразно ориентироваться на данные предварительно собранного ритма спонтанных мочеиспусканий. На протяжении трех дней ребенок без напоминаний, по собственному желанию мочится в горшок. Родители записывают число мочеиспусканий и объем каждой порции мочи. Именно средний объем мочи при мочеиспускании должен учитываться при введении количества контрастного вещества в мочевой пузырь. В классическом варианте цистоуретрография предусматривает выполнение двух снимков. Первый после введения контрастного вещества до ощущения позыва. Оценивая первый снимок рентгенологи исключают пассивный пузырно-мочеточниковый рефлюкс. Второй снимок выполняют при микции в повороте ребенка в три четверти, для лучшей визуализации мочеиспускательного канала. Заброс мочи в мочеточник или лоханку при микции свидетельствует о наличии активного ПМР.
При обследовании больных с подозрением на ПМР обращают пристальное внимание на состояние верхних отделов мочевой системы (почки и мочеточники). Ультразвуковое исследование с измерением размеров чашечек, лоханки, паренхимы и мочеточника с оценкой кровотока паренхимы почки с помощью цветового картирования позволяет получить общее представление о состоянии почек. Экскреторная урография при ПМР указывает на степень сохранности функции почек, размерах ЧЛС и форме мочеточников. Поздние снимки при опорожненном мочевом пузыре дают информацию о сократительной способности мочеточников и проходимости пиелоуретерального и уретеровезикального сегментов. Радиоизотопное исследование при ПМР, проводится в динамике, позволяет оценить по функции почек эффективность консервативного лечения. Прогрессирующий нефросклероз при ПМР наряду с инфекцией мочевых путей и сохраняющимся ПМР (либо увеличивающаяся степень ПМР), считается определяющим фактором для проведения хирургических вмешательств.
Отдельным пациентам целесообразно проведение цистоуретроскопии. Состояние устьев, их размер, форма, степень смыкания, длина подслизистого туннеля (Рис. 5)
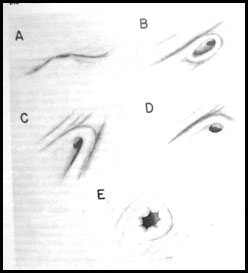 | А- нормальное 4% В- в виде стадиона 28% С- подковообразное Д- латеральное 83% Е - в виде лунки для гольфа 100% |
| Рис.5 Варианты формы устья мочеточника |
Трабекулярность или признаки воспаления слизистой мочевого пузыря могут влиять на выбор тактики и метода лечения. Трабекулярность слизистой подтверждает наличие нейрогенных дисфункций мочевого пузыря или детрузорно-сфинктерную диссенергию, наряду с признаками цистита данные изменения требуют предварительной медикаментозной терапии и физиолечения. Дети с учащенным мочеиспусканием, императивными позывами, недержанием мочи должны пройти обязательное уродинамическое обследование включающее ритм спонтанных мочеиспусканий, цистометрию, урофлоуметрию.
Неоперативное лечение ПМР эффективно в большинстве случаев и состоит из четырех этапов: 1) диагностика, 2) профилактика инфекции, 3) лечение функциональных нарушений мочеиспускания и 4) наблюдение за больным. Диагностика была описана выше. Следует подчеркнуть, что при ПМР абсолютно необходимо исключить функциональные нарушения мочеиспускания и обструкцию выходного отдела мочевого пузыря, а при их выявлении проводить соответствующее лечение. Пациенты, у которых есть подозрения на непроизвольные сокращения детрузора, должны получать супрессивную терапию. С этой целью в большинстве случаев рекомендуется применять у детей оксибутинин (oxibutinin hydrochlorid) C.A.Sheldon (1997).Нейровезикальная дисфункция с задержками мочи может потребовать периодической катетеризации мочевого пузыря.
Применяются следующие виды оперативных вмешательств : субтригональная инъекция (эндоскопическое введение болюса коллагена, уродекса, вантриса или инертного вещества под устье в треугольнике Льето). (Рис.6) и открытые операции:
экстравезикальная детрузорорафия ( укладка мочеточника в подслизистый слой без рассечения просвета мочевого пузыря) Грегуар,Hutch; интрапузырное продвижение мочеточника (Cohen, Politano-Leadbetter)(Рис.7).
 |
| Рис.6. Эндоскопическое лечение рефлюкса пункционное введение объемобразующего вещества в подслизистый слой мочеточника (в результате устье смыкается) |
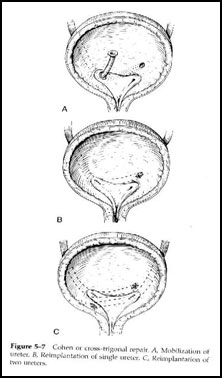 |
| Рис.7 Открытые операции по лечению ПМР Уретероцисто-неоимплантацияс антирефлюксной защитой по Cohen |
Выбор метода лечения зависит от множества факторов и проводится индивидуально в каждом конкретном случае. Эффективность лечения ПМР зависит от полноты обследования, выявления всех факторов способствующих возникновению ПМР и рационально подобранному консервативному лечению, либо оптимальному методу оперативной коррекции. Сегодня помимо открытых операций мы широко используем лапароскопическую реимплантацию мочеточника по экстравезикальной методике
Доктор Рудин Ю.Э.
Тел. 499-164-13-65
www.drrudin.ru
Рефлюкс мочеточника или пузырно-мочеточниковый рефлюкс (ПМР) – это патологическое состояние, которое характеризуется обратным оттоком урины из мочевого пузыря в почки. Появление такого нарушения обусловлено недостаточной степенью закрытия устья мочеточника в процессе наполнения мочевого пузыря или при мочеиспускании. На фоне ПМР часто отмечаются хронические воспалительные процессы в органах мочевыделительной системы, повреждение почечной ткани, развитие рефлюкс-нефропатии, повышение давления.

Эти осложнения при отсутствии адекватного лечения и устранения их причины могут привести к серьезным последствиям для организма. В большинстве случаев рефлюкс мочеточника встречается в детском возрасте, что связано с врожденными патологиями развития данного трубчатого органа.
Причинами рефлюкса мочеточников чаще всего являются различные аномалии их развития в процессе эмбриогенеза. Однако бывают случаи, когда появление заболевания обусловлено вторичными факторами. К ним относятся воспалительные процессы в органах мочевой системы, последствия операций на мочевом пузыре и др.Среди первичных причин возникновения ПМР наиболее часто отмечаются:
К вторичным факторам развития ПМР относятся следующие заболевания, в результате которых возникают препятствия для нормального пассажа мочи:
Важно: Мочеточник представляет собой полый трубчатый орган, длина которого составляет от 25 до 30 см, а внутренний диаметр 6–8 мм.
Рефлюкс мочеточника бывает транзиторным и постоянным. В первом случае он возникает только в период обострений хронических воспалительных заболеваний (цистит, простатит), а во втором – присутствует всегда. В зависимости от того, при каких процессах возникает ПМР, различают:
ПМР может протекать с различной степенью тяжести:

Степени пузырно-мочеточникового рефлюкса
Симптомы ПМР бывает трудно идентифицировать, в связи с чем заболевание часто обнаруживается уже при развитии осложнений. Недостаток массы тела при рождении, отставание в физическом развитии, нарушенная функция мочевого пузыря у детей могут свидетельствовать о наличии у них рефлюкса мочеточника.К наиболее характерным признакам ПМР относятся:
Совет: При выявлении любых нарушений в работе мочевыводящей системы следует обратиться к врачу для установления их причины.
Диагноз ПМР можно подтвердить при помощи микционной цистоуретрографии. Это исследование заключается во введении в мочевой пузырь через специальный катетер контрастного вещества и последующем выполнении серии рентгенограмм (цистограмм) во время заполнения и опорожнения пузыря. Если рефлюкс мочеточника сопровождается воспалительным процессом, то цистоуретрографию необходимо проводить только спустя 7 дней после снятия воспаления.

Цистограмма при активном ПМР
Для выяснения причины, спровоцировавшей возникновение заболевания, могут применяться:
Применяемые методы лечения ПМР направлены на ликвидацию причины патологии и профилактику осложнений. Одним из наиболее тяжелых последствий является рефлюкс-нефропатия, представляющая собой деструктивный воспалительный процесс в паренхиме почек. Для лечения ПМР в зависимости от тяжести его течения и причины возникновения патологии могут применяться консервативные или хирургические методы.
Консервативное лечение оказывается достаточно эффективным на ранних стадиях заболевания. У детей в некоторых случаях ПМР может исчезнуть самостоятельно. Главная цель консервативной терапии заключается в профилактике и своевременном лечении инфекций мочевыделительной системы.В клинической практике применяются следующие подходы к лечению ПМР:
Хирургические методы устранения ПМР показаны пациентам в следующих случаях:
Среди оперативных методов лечения рефлюкса мочеточника применяются создание нового устья или введение биоимплантов, способствующих эффективному смыканию устья. В большинстве случаев при сохранении сократительной способности устья хирургическое вмешательство может быть произведено эндоскопическим методом.

Эндоскопическая коррекция рефлюкса мочеточника путем введения биоимпланта под внутрипузырный отдел
Рекомендация: Для предупреждения развития и прогрессирования ПМР необходимо своевременно лечить воспалительные заболевания мочевой системы и обращаться к врачу при любых нарушениях акта мочеиспускания. Чтобы снизить риск врожденных пороков мочеточников у будущего ребенка, женщина должна придерживаться здорового питания и образа жизни.
Рекомендуем прочитать историю Ольги Кировцевой, как она вылечила желудок... Читать статью >>
Оценка статьи:
 Загрузка...
Загрузка... Поделиться с друзьями:
Все материалы на сайте ozhivote.ru представленыдля ознакомления, возможны противопоказания, консультация с врачом ОБЯЗАТЕЛЬНА! Не занимайтесь самодиагностикой и самолечением!
ozhivote.ru